用在P+CuSO4+H2O---Cu3p+H3PO4+H2SO4(未配平)的反应中 7.5molCuSO4可氧化P的物质
来源:学生作业帮 编辑:大师作文网作业帮 分类:化学作业 时间:2024/10/07 19:21:10
用在P+CuSO4+H2O---Cu3p+H3PO4+H2SO4(未配平)的反应中 7.5molCuSO4可氧化P的物质的量为?
详解,电子转移守恒到底怎么做?
详解,电子转移守恒到底怎么做?
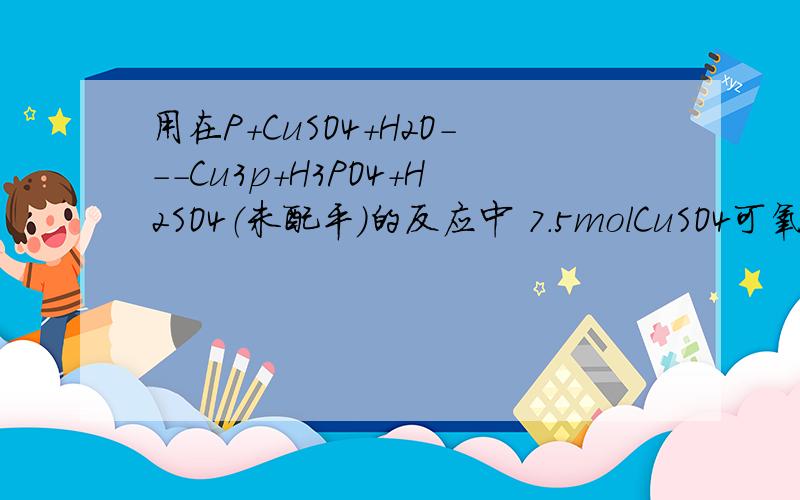
P+CuSO4+H2O---Cu3P+H3PO4+H2SO4
Cu +2->+1得到电子e*3
P 0->-3 得到电子3e
P 0->+5失去电子5e
得失电子相等,即(e*3+3e)*5=5e*6
则11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4
7.5molCuSO4中Cu +2->+1得到电子7.5mole可氧化n(P)=7.5mole/5e=1.5mol
注:P 0->+5失去电子5e才作为被氧化的P元素
得失电子过程与化学配平需要注意产物的原子个数
Cu +2->+1得到电子e*3
P 0->-3 得到电子3e
P 0->+5失去电子5e
得失电子相等,即(e*3+3e)*5=5e*6
则11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4
7.5molCuSO4中Cu +2->+1得到电子7.5mole可氧化n(P)=7.5mole/5e=1.5mol
注:P 0->+5失去电子5e才作为被氧化的P元素
得失电子过程与化学配平需要注意产物的原子个数
在P+CuSO4+H2O → Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物
11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4反应中,被氧化的P原子与被还原的P原子个数比
P+CuSO4+H2O=Cu3P+H3PO4+H2SO4
P+CuSO4+H2O=Cu3P+H2SO4+H3PO4中哪个是氧化剂,哪个是还原剂,是怎么判断的?
白磷与硫酸铜反应,用氧化还原的知识怎么配平?P4+CuSO4+H2O=Cu3P+H3PO4+H2SO4
P+CuSO4+H2O→Cu3P+H3PO4+H2SO4怎样配平的?用化合价升降法.要分析过程.
方程式配平P+CuSO4+H2O→Cu3P+H3PO4+H2SO4
P+CuSO4+H2O=Cu3P+H3PO4+H2SO4如何配平?
配平一个化学方程式:()P+()CuSO4+()H2O=()Cu3P+()H3PO4+()H2SO4
P+CuSO4+H2O=Cu3P+H2So4+H2Po4的配平
请根据反应15 CuSO4+11 P+24 H2O=5 Cu3P+6 H3PO4+15 H2SO4 ,判断1mol硫酸铜
P4+ CuSO4+ H2O— Cu3P+ H2SO4+ H3PO4