Ksp(AgCl)>Ksp(Ag2CrO4),那么把相同物质的量浓度的AgNO3(aq)加入KCl(aq)和K2CrO4
来源:学生作业帮 编辑:大师作文网作业帮 分类:化学作业 时间:2024/09/26 01:29:07
Ksp(AgCl)>Ksp(Ag2CrO4),那么把相同物质的量浓度的AgNO3(aq)加入KCl(aq)和K2CrO4(aq),先产生什么沉淀?
先产生什么沉淀?为什么?是不是先产生更易溶的沉淀?请给予解释。
先产生什么沉淀?为什么?是不是先产生更易溶的沉淀?请给予解释。
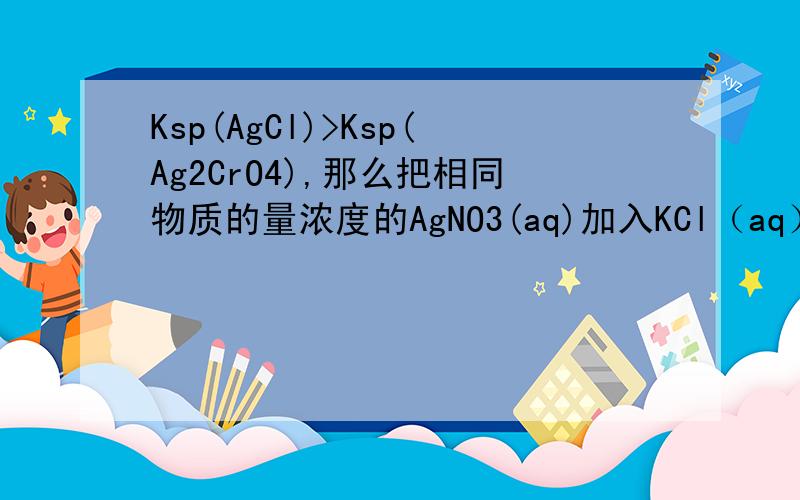
AgCl恰好沉淀时:[Ag+]₁=Ksp(AgCl)/[Cl-]
Ag2CrO4恰好沉淀时:[Ag+]₂=√Ksp(Ag2CrO4)/[CrO42-]
当[Ag+]₁≥[Ag+]₂时:
Ksp(AgCl)/√Ksp(Ag2CrO4)≥[Cl-]/√[CrO42-]
即当满足上式时,Ag2CrO4先沉淀,否则AgCl先沉淀
实际上是溶解度小的先沉淀.
但是注意一点,当沉淀的类型不一样时,不能直接利用Ksp判定溶解度.比如本题的Ag2CrO4和AgCl,前者是A2B类型,后者是AB类型,两者类型不一样,所以不能用Ksp判定溶解度,而必须通过计算.
Ag2CrO4恰好沉淀时:[Ag+]₂=√Ksp(Ag2CrO4)/[CrO42-]
当[Ag+]₁≥[Ag+]₂时:
Ksp(AgCl)/√Ksp(Ag2CrO4)≥[Cl-]/√[CrO42-]
即当满足上式时,Ag2CrO4先沉淀,否则AgCl先沉淀
实际上是溶解度小的先沉淀.
但是注意一点,当沉淀的类型不一样时,不能直接利用Ksp判定溶解度.比如本题的Ag2CrO4和AgCl,前者是A2B类型,后者是AB类型,两者类型不一样,所以不能用Ksp判定溶解度,而必须通过计算.
向Ag2CrO4悬浊液中加入NaCl溶液 有AgCl沉淀生成 能确定Ksp(AgCl)与Ksp(Ag2CrO4)的大小吗
已知Agcl在水中存在沉淀溶解平衡:Agcl(s)=Ag+(aq)+cl -(aq).在25℃时,氯化银的Ksp=1.8
AgCl(s) Ag+(aq)+ Cl-(aq) Ksp=c(Ag+) × c(Cl-) 为什么Ksp不用除c(AgCl
Ksp和aq都知道Ksp是离子积浓度,aq是离子状态.Kw是水的离子积常数,因为w是water的首字母.那上述这两个单词
沉淀-溶解平衡已知室温下AgCl的Ksp = 1.8×10*-10,Ag2CrO4的 Ksp = 1.9×10*-12,
已知在室温下AgCL的Ksp=1.8×10^-10,Ag2CrO4的Ksp=1.1×10^-12
已知在室温下AgCL的Ksp=1.8×10^-10,Ag2CrO4的Ksp=1.1×10^-12,
沉淀溶解平衡19,在2mL物质的量浓度相等的和NaI溶液中滴入几滴AgNO3溶液,发生的反应为( )(已知Ksp(AgI
已知Ksp(Agcl)=1.56*10^-10,Ksp(AgBr)=7.7*10^-13,Ksp(Ag2CrO4)=9.
把100g某NaOH(aq)(密度=1.22g/ml)蒸发浓缩余下50ml(aq)时,物质的量浓度为8mol/L.求原溶
已知25℃时,AgCl的Ksp=1.8*10^-10.将足量的AgCl加入100ml0.3mol/L的AgNO3溶液中
沉淀溶解平衡问题就是那个Ksp,举个例子Ksp[AgCl]=c(Ag+)*c(Cl-),这里的银离子浓度和氯负离子浓度指