298K时,在Fe3+,Fe2+的混合溶液中加入NaOH时,有Fe(OH)3,Fe(OH)2沉淀生成(假设无其它反应发生
来源:学生作业帮 编辑:大师作文网作业帮 分类:数学作业 时间:2024/09/22 07:05:52
298K时,在Fe3+,Fe2+的混合溶液中加入NaOH时,有Fe(OH)3,Fe(OH)2沉淀生成(假设无其它反应发生).当沉淀反应达到平衡,并保持c(OH-)=1.0mol·L-1时.求E θ{Fe(OH)3/Fe(OH)2}=?
为什么 c(OH-)=1.0mol·L-1时,
E (Fe3+/Fe2+)就是电极反应Fe(OH)3 + e Fe(OH)2+OH-的标准电极电势 E θ{Fe(OH)3/Fe(OH)2}
真的很晕,希望详解,
为什么 c(OH-)=1.0mol·L-1时,
E (Fe3+/Fe2+)就是电极反应Fe(OH)3 + e Fe(OH)2+OH-的标准电极电势 E θ{Fe(OH)3/Fe(OH)2}
真的很晕,希望详解,
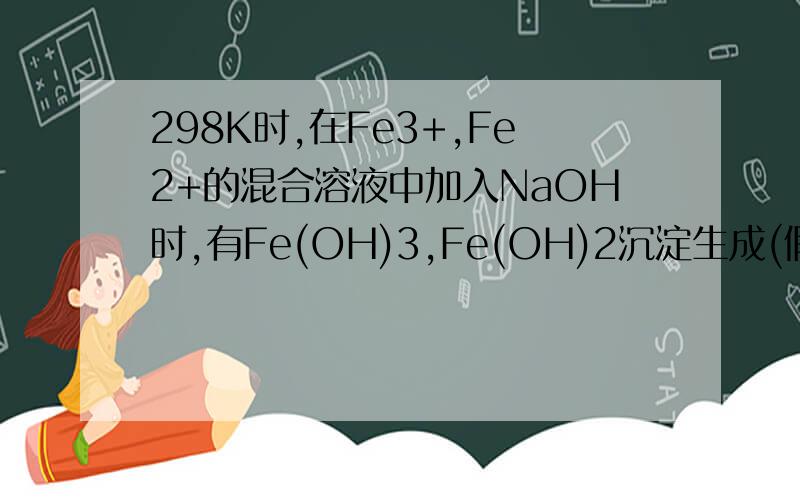
先把此题Nernst方程写出来,然后你会发现在表达式里的lg上有一项OH-的浓度,既然是算标准电极电势,当然要所有离子的浓度都是1mol/L,这样就相当于乘了一个1而不会因OH-浓度影响结果了.
不明白的可以继续问~
再问: 那为什么E (Fe3+/Fe2+)等于E θ{Fe(OH)3/Fe(OH)2} 呀 谢谢你
再答: 这是从数学表达式里得到的结论。其实你也可以这么想,只不过不是很严谨。如果还原态生成沉淀,那么电势会增高,如果氧化态生成沉淀,那么电势会降低。此例恰好氧化态还原态均生成沉淀,效果抵消,所以就等于没变。
不明白的可以继续问~
再问: 那为什么E (Fe3+/Fe2+)等于E θ{Fe(OH)3/Fe(OH)2} 呀 谢谢你
再答: 这是从数学表达式里得到的结论。其实你也可以这么想,只不过不是很严谨。如果还原态生成沉淀,那么电势会增高,如果氧化态生成沉淀,那么电势会降低。此例恰好氧化态还原态均生成沉淀,效果抵消,所以就等于没变。
4、298k时,在Fe3+、Fe2+的混合溶液中加入NaOH溶液时,有Fe(OH)3、Fe(OH)2沉淀生成(假设无其他
假设溶液中Fe3+离子浓度为0.2mol/l,则开始生成Fe(OH)3沉淀的PH是多少?沉淀完全的PH是多少?
盐类水解的问题.Fe3+,在沸水中反应生成Fe(OH)3胶体的反应.离子方程式为Fe3+ +3h2o 加热= Fe(oh
当存在FE3+,CU2+,FE,时 先发生的反应是FE+FE3+=3Fe2+,FE+CU2+=CU+FE2+ CU+2F
将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤 C..
溶液中含有Fe2+和Fe3+浓度均为0,1mol/l如果要求Fe(OH)3定性沉淀完全,而Fe(OH)2不沉淀,需要控制
一种溶液中含有Fe3+和Fe2+,它们的浓度均为0.05mol/l,如果只要求Fe(OH)3沉淀,需控制pH的范围
若溶液中含有杂质fe3+和fe2+,采用沉淀的最好方式a.feco3 b.fe(oh)2 c.f
除废水中的Fe2+时,Fe2+变成Fe3+后,调节pH至3.7,然后Fe(OH)3沉淀是怎么出来的?
Fe(OH)3胶体中加入Mg(OH)2溶液会有红褐色沉淀析出,为什么它是物理变化啊?
1.FeCl3与NaOH反应生成的是Fe(OH)3胶体还是沉淀,为什么
证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 向2 mL 1 mol/L NaOH溶液中先加入3滴1 mol/L