已知3Mg+N2=Mg2N2; Mg2N2+6H2o=3Mg(OH)2+2NH3 (1) 1.2g镁完全反应转移的电子数
来源:学生作业帮 编辑:大师作文网作业帮 分类:化学作业 时间:2024/09/21 03:26:13
已知3Mg+N2=Mg2N2; Mg2N2+6H2o=3Mg(OH)2+2NH3 (1) 1.2g镁完全反应转移的电子数是多少 2) (
2) (1.2g镁按上方程式完全反应后,可以得到STP条件下NH3的体积是多少
2) (1.2g镁按上方程式完全反应后,可以得到STP条件下NH3的体积是多少
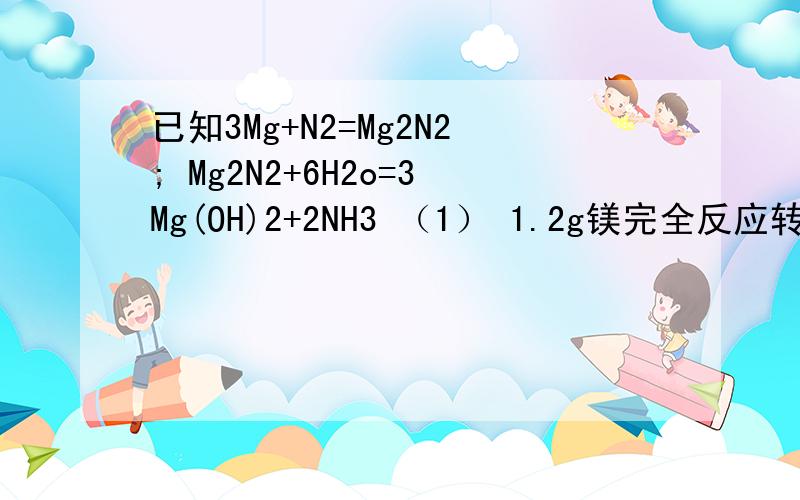
1.1.2g Mg的物质的量是n=m/M=1.2/24=0.05mol
1个Mg最外层有2个电子,所以转移电子的物质的量是0.05*2=0.1mol,即0.1NA个.
2.由3Mg+N2=Mg2N2、Mg2N2+6H2O=3Mg(OH)2+2NH3可以得到关系式
3 2
0.05mol n(NH3)
n(NH3)=0.033mol
NH3的体积是V=n*Vm=0.033*22.4=0.74L
答:(1) 1.2g镁完全反应转移的电子数是0.1NA
(2)1.2g镁按上方程式完全反应后,可以得到STP条件下NH3的体积是0.74L.
1个Mg最外层有2个电子,所以转移电子的物质的量是0.05*2=0.1mol,即0.1NA个.
2.由3Mg+N2=Mg2N2、Mg2N2+6H2O=3Mg(OH)2+2NH3可以得到关系式
3 2
0.05mol n(NH3)
n(NH3)=0.033mol
NH3的体积是V=n*Vm=0.033*22.4=0.74L
答:(1) 1.2g镁完全反应转移的电子数是0.1NA
(2)1.2g镁按上方程式完全反应后,可以得到STP条件下NH3的体积是0.74L.
下列物质中,碱性最强的是KOH、Mg(OH)2、NH3、H2O、Al(OH)3、
【急】关于“Mg+H2O=Mg(OH)2+H↑”一反应的问题.
一道电子数转移题6NO+4NH3=5N2+6H2O.若有3.6g水生成.则转移电子数为?
镁与热水的反应方程式为:MG+2H2O=MG(OH)2+H2I,MG(OH)2不是沉淀吗?为什么没有沉淀符号?
NaNO2+NH4Cl=NaCl+N2+2H2O 为什么生成1molN2时转移的电子数为3mol
镁在空气中生成氧化镁和化合物M,M能与水发生如下反应:M+6H2O═3Mg(OH)2+2NH3↑,则M的化学式为( )
Mg+2H2O=Mg(OH)2+H2 属于什么基本反应类型?
Mg+H2O=Mg(OH)2+H↑ Mg(OH)2要写沉淀符号吗
2H2O+Mg=====Mg(OH)2+H2↑ Mg(OH)2加↓不
Mg + 2H2O == Mg(OH)2 + H2 ,为什么Mg(OH)2不要打沉淀符号?
Mg(oh)2与h2o反应么
Mg+2H2O(沸水)=加热 Mg(oH)2+H2箭头向上 为什么Mg(oH)2不用标箭头