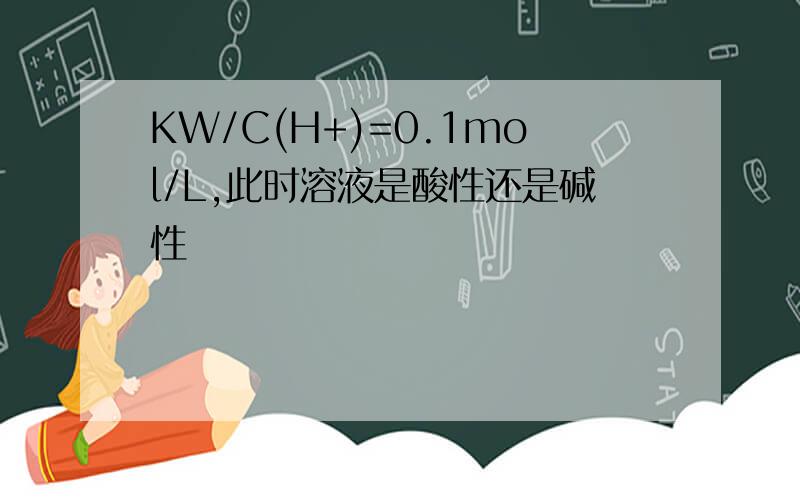
KW/C(H+)=0.1mol/L,此时溶液是酸性还是碱性
c(H+)=0.1mol.L-1说明什么溶液是酸性还是碱性的啊
水电离出的c(h^+)=1×10^-12mol/l的溶液是酸性还是碱性?为什么?
水电离出的c(h^+)=1×10^-13mol/l的溶液是酸性还是碱性?为什么?
0.02mol/L硫酸还是c(h+)=0.1mol/L的溶液 酸性比较强?
++急求++ 由水电离的c(H+)=10^-12mol/L的溶液酸性还是碱性?
常温下,由水电离产生的C(OH-)=0.1mol/l的溶液中 是酸性溶液还是碱性溶液,怎样判断
由水电离出来的C(H+)=1*10^-13mol/L的溶液为什么有可能是碱性也有可能是酸性?
1、某溶液中由水电离产生的c(H+) H2O= 10-12 mol/L ,则该溶液呈酸性还是碱性?并求算该溶液中 c(H
为什么水电离出的c(H+) = 1 ×10-3mol/L,此时溶液可能显酸性?
为什么说“比如溶液中由水电离生成的c(H+)=10-12mol·L-1”的溶液可能呈酸性也可能显碱性?
常温下,由水电离出的c(H+)=10-14mol/L的溶液,可能是pH为14的碱性溶液或pH为0的酸性溶液
0.01mol/L的醋酸钠与0.02mol/L的醋酸等体积混合,溶液是酸性还是碱性