高中化学题某温度下,0.1mol•L-1NaHCO3溶液pH=10,下列判断正确的是
来源:学生作业帮 编辑:大师作文网作业帮 分类:化学作业 时间:2024/09/22 01:06:59
高中化学题某温度下,0.1mol•L-1NaHCO3溶液pH=10,下列判断正确的是
A.c(OH-)=10-4mol·L-1
B.加入少量NaOH固体,c(Na+)和c(HCO3-)均增大
C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)
D.c(Na+)=c(HCO3-)+ c(CO32-) +c(H2CO3)
A.c(OH-)=10-4mol·L-1
B.加入少量NaOH固体,c(Na+)和c(HCO3-)均增大
C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)
D.c(Na+)=c(HCO3-)+ c(CO32-) +c(H2CO3)
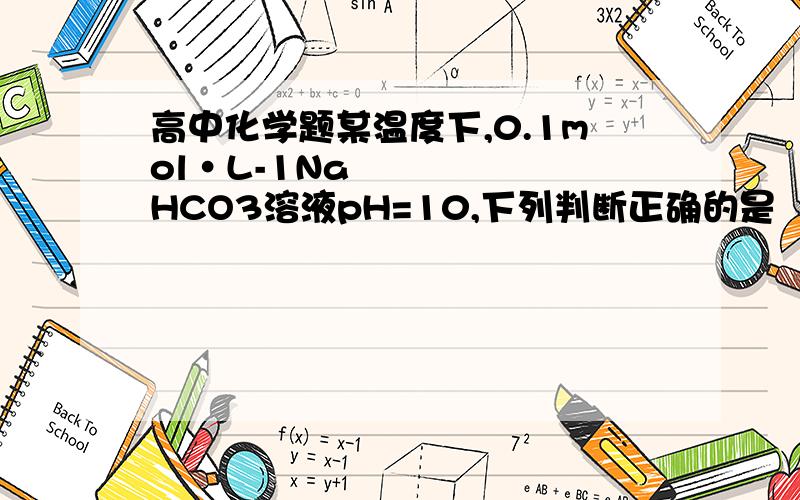
A.c(OH-)=10-4mol·L-1
错.没说温度?pH=10.POH=?-10
B.加入少量NaOH固体,c(Na+)和c(HCO3-)均增大
错 会先反应的.HCO3-浓度减小!Na+浓度增大
C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)
错 缺少CO32-,电荷不守恒的!
D.c(Na+)=c(HCO3-)+ c(CO32-) +c(H2CO3)
对的,物料守恒(Na+与C原子比例为1:1)
错.没说温度?pH=10.POH=?-10
B.加入少量NaOH固体,c(Na+)和c(HCO3-)均增大
错 会先反应的.HCO3-浓度减小!Na+浓度增大
C.c(Na+)+c(H+)=c(HCO3-)+c(OH-)
错 缺少CO32-,电荷不守恒的!
D.c(Na+)=c(HCO3-)+ c(CO32-) +c(H2CO3)
对的,物料守恒(Na+与C原子比例为1:1)
高中化学题某温度下,0.1mol•L-1NaHCO3溶液pH=10,下列判断正确的是
高中化学题,对于0.1mol•L-1 Na2CO3溶液,正确的是( ) A.略升高温度,溶液
常温下,0.1mol/l 某一元酸(HA)溶液中pH=2,下列叙述正确的是( )
某温度下,0.1mol/L醋酸溶液的PH=3.
0.1mol/L NaHCO3的溶液的PH最接近于:
室温下,取0.3mol/l HY溶液与0.3mol/lNaOH溶液等体积混合,测得ph=9,则下列正确的是
常温下0.1mol•L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
某温度下纯水中C(H+) = 2×10-7 mol/L,0.9mol/L氢氧化钠与0.1mol/L盐酸混合后溶液pH为多
某温度下,0.1mol/L醋酸溶液的ph=3.将该温度下0.2mol/L醋酸溶液和0.2mol/L醋酸钠溶液等体积混合后
已知0.01mol/l 二元酸H2A溶液的PH=4,下列说法正确的是
某温度下0.1mol/L的NaHB溶液中ph
取20mL NaHCO3溶液于锥形瓶中,用0.1mol/L盐酸滴定.滴定过程中,混合液pH的变化如图所示.下列叙述正确的