化学离子浓度题25摄氏度,将0.15 mol/L稀硫酸V1 mL与0.1 mol/L NaOH溶液V2 mL混合,所得溶
来源:学生作业帮 编辑:大师作文网作业帮 分类:化学作业 时间:2024/09/24 01:22:47
化学离子浓度题
25摄氏度,将0.15 mol/L稀硫酸V1 mL与0.1 mol/L NaOH溶液V2 mL混合,所得溶液的pH为1,
则V1∶V2=________.(溶液体积变化忽略不计)
(2)常温下,某水溶液中存在的离子有:Na+
、A-
、H+
、OH-
,根据题意,回答下列问题:①若由0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合而得,则溶液的pH______7.②若溶液
pH>7,则
c(Na
+
)__________c(A
-
),理由是
______________________________.
③若溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合而得,则下列说法正确的是________(填选项代号).
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol/L
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
25摄氏度,将0.15 mol/L稀硫酸V1 mL与0.1 mol/L NaOH溶液V2 mL混合,所得溶液的pH为1,
则V1∶V2=________.(溶液体积变化忽略不计)
(2)常温下,某水溶液中存在的离子有:Na+
、A-
、H+
、OH-
,根据题意,回答下列问题:①若由0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合而得,则溶液的pH______7.②若溶液
pH>7,则
c(Na
+
)__________c(A
-
),理由是
______________________________.
③若溶液由pH=3的HA溶液V1 mL与pH=11的NaOH溶液V2 mL混合而得,则下列说法正确的是________(填选项代号).
A.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol/L
B.若V1=V2,反应后溶液pH一定等于7
C.若反应后溶液呈酸性,则V1一定大于V2
D.若反应后溶液呈碱性,则V1一定小于V2
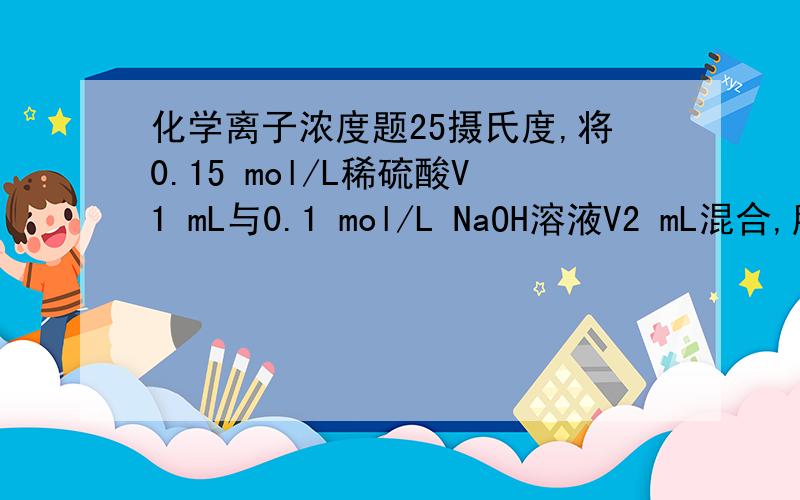
(1)1∶1 (2)①大于或等于
②大于根据电荷守衡,c(H+)+c(Na+)=c(OH-)+c(A-),由于c(OH-)>c(H+),故c(Na+)>c(A-)
③B C
解析:(1)H2SO4+2NaOH====Na2SO4+2H2O
=10-1
mol·L-1
解得V1=V2
∴V1∶V2=1∶1.
(2)中①所得溶液中溶质仅有NaA,其若为强碱强酸盐,溶液pH=7;若为强碱弱酸盐,水解显碱性,溶液pH>7.②问,由pH>7,可知c(OH-)>c(CH+),再由电荷守恒知c(Na+)+c(H+)=c(OH-)+c(A-),则c(Na+)>c(A-).③问,常温中性溶液中c(H+)=c(OH-)=1×10-7
mol·L-1,则c(H+)+c(OH-)=2×10-7
mol·L-1,A项说法正确.当HA为弱酸时,若V1=V2,反应后HA过量,所得溶液呈酸性,pH<7,B、C两项说法都不正确.HA可能是强酸,也可能是弱酸,c(HA)≥c(H+)=10-pH
mol·L-1=10-3
mol·L-1,而c(NaOH)=c(OH-)=10pH-14
mol·L-1=10-3
mol·L-1,若要混合液呈碱性,NaOH溶液必须过量,则V1一定小于V2,D项说法正确.
②大于根据电荷守衡,c(H+)+c(Na+)=c(OH-)+c(A-),由于c(OH-)>c(H+),故c(Na+)>c(A-)
③B C
解析:(1)H2SO4+2NaOH====Na2SO4+2H2O
=10-1
mol·L-1
解得V1=V2
∴V1∶V2=1∶1.
(2)中①所得溶液中溶质仅有NaA,其若为强碱强酸盐,溶液pH=7;若为强碱弱酸盐,水解显碱性,溶液pH>7.②问,由pH>7,可知c(OH-)>c(CH+),再由电荷守恒知c(Na+)+c(H+)=c(OH-)+c(A-),则c(Na+)>c(A-).③问,常温中性溶液中c(H+)=c(OH-)=1×10-7
mol·L-1,则c(H+)+c(OH-)=2×10-7
mol·L-1,A项说法正确.当HA为弱酸时,若V1=V2,反应后HA过量,所得溶液呈酸性,pH<7,B、C两项说法都不正确.HA可能是强酸,也可能是弱酸,c(HA)≥c(H+)=10-pH
mol·L-1=10-3
mol·L-1,而c(NaOH)=c(OH-)=10pH-14
mol·L-1=10-3
mol·L-1,若要混合液呈碱性,NaOH溶液必须过量,则V1一定小于V2,D项说法正确.
化学离子浓度题25摄氏度,将0.15 mol/L稀硫酸V1 mL与0.1 mol/L NaOH溶液V2 mL混合,所得溶
将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合
20 mL 1mol/L的HAc与40 mL 0.5mol/L的NaOH混合后,所得溶液中离子浓度由大到小的顺序为( )
100mL 0.1 mol/L CH3COOH与50mL 0.2 mol/L NaOH溶液混合,在所得溶液中( )
将5ml 0.2mol/l HAC溶液与10ml 0.1mol/l KOH溶液相混合,所得溶液中微粒浓度相对大小顺序是(
将 0.6mol/L 的硫酸溶液 100mL 与 0.2mol/L 的硫酸溶液 400mL 相混合,所得混合溶液 的物质
混合溶液离子浓度比较将20ml 0.4mol/L硝酸铵溶液跟50ml 0.1mol/L氢氧化钡溶液混合,则溶液中个离子浓
20mL 0.1mol/L的硫酸与5mL 0.1mol/L的硫酸混合,求混合后硫酸溶液物质的量浓度.
将5ml 0.4mol/L AgNO3 溶液与10ml 0.3mol/L BaCl2 溶液混合,反应后溶液中离子浓度最大
化学"300ml 0.5mol/l naoh 与200ml 0.4mol/l 的h2so4混合
100ml 0.1mol 醋酸与50ml 0.2mol NaOH溶液混合,所得溶液中的歌离子浓度大小(要解析)
将0.1mol的镁、铝混合物溶于100mL 3 mol/L NAOH溶液中充分反应,再加入1mol/L硫酸溶液120ml