2.已知:H+(aq) + OH-(aq) → H2O(l) + 57.3 kJ.对于下列反应:
来源:学生作业帮 编辑:大师作文网作业帮 分类:化学作业 时间:2024/09/23 08:20:14
2.已知:H+(aq) + OH-(aq) → H2O(l) + 57.3 kJ.对于下列反应:
①HCl(aq) + NH3•H2O(aq) → NH4Cl(aq) + H2O(l) + a kJ
②HCl(aq) + NaOH(s) → NaCl(aq) + H2O(l) + b kJ
③HNO3(aq) + KOH(aq) → KNO3(aq) + H2O(l) + c kJ
则a、b、c三者的大小关系为 ( )
A.a>b>c B.b>c>a C.a=b=c D.无法比较
我选的是A为什么错啊 我是这样考虑的 ①的左边都是气态右边气态和液态②的左边是气态和液态 右边和①一样是气态液态 那d得到a放热》b选A为啥米错丫?
①HCl(aq) + NH3•H2O(aq) → NH4Cl(aq) + H2O(l) + a kJ
②HCl(aq) + NaOH(s) → NaCl(aq) + H2O(l) + b kJ
③HNO3(aq) + KOH(aq) → KNO3(aq) + H2O(l) + c kJ
则a、b、c三者的大小关系为 ( )
A.a>b>c B.b>c>a C.a=b=c D.无法比较
我选的是A为什么错啊 我是这样考虑的 ①的左边都是气态右边气态和液态②的左边是气态和液态 右边和①一样是气态液态 那d得到a放热》b选A为啥米错丫?
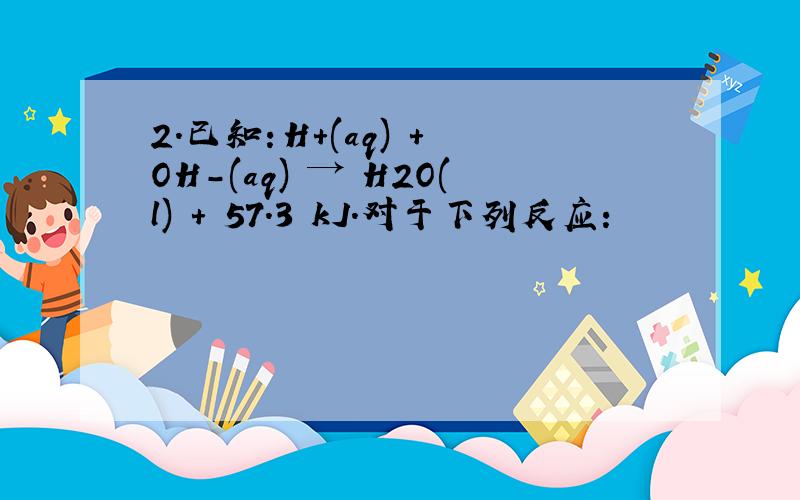
B.b>c>a
①HCl(aq) + NH3•H2O(aq) → NH4Cl(aq) + H2O(l) + a kJ
NH3.H2O---弱碱,电离吸热,放热少!
②HCl(aq) + NaOH(s) → NaCl(aq) + H2O(l) + b kJ
NaOH(s)---多放出熔解热!
③HNO3(aq) + KOH(aq) → KNO3(aq) + H2O(l) + c kJ
①HCl(aq) + NH3•H2O(aq) → NH4Cl(aq) + H2O(l) + a kJ
NH3.H2O---弱碱,电离吸热,放热少!
②HCl(aq) + NaOH(s) → NaCl(aq) + H2O(l) + b kJ
NaOH(s)---多放出熔解热!
③HNO3(aq) + KOH(aq) → KNO3(aq) + H2O(l) + c kJ
2.已知:H+(aq) + OH-(aq) → H2O(l) + 57.3 kJ.对于下列反应:
.已知H+(aq)+OH-(aq)=H2O(l);△H=-57.3 kJ/mo
已知热化学方程式:H+(aq)+OH-(aq)=H2O(l),△H1=-57.3KJ/mol
强酸与强碱发生中和反应的热化学方程式为:H+(AQ)+OH-(AQ)=H2O(l),△H=-57.3kj/mol,下列实
.下列有关H+(aq)+OH-(aq) H2O(l);ΔH=-57.3 kJ/mol的离子反应的说法正确的是 ( )
下列有关H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol的离子反应说法正确的是( )
已知H+(aq)+OH-(aq)==H2O(l) △H=-+57.3kJ/mol 则中和热的热效应均为57.3kj
已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ/mol,则下列说法中正确的是(
已知298K时,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,推测含1mol H
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol,
已知:H+(aq)+OH-(aq)=H2O(l);ΔH=-57.3
表示中和热的离子方程式为:H+(aq)+OH-(aq)=H2O(l) H=-57.3kj/mol-1